君实又一重磅授权,特瑞普利如何拓宽出海路?
5月5日晚,君实生物发布公告,宣布与瑞迪博士实验室签署《独占许可与商业化协议》,同意向瑞迪博士实验室授予许可,于巴西、墨西哥、哥伦比亚、阿根廷、秘鲁、智利、巴拿马、乌拉圭、印度及南非开发及独占地商业化特瑞普利单抗注射液。瑞迪博士实验室可选择将许可范围扩大至涵盖澳大利亚及新西兰以及其他9个国家。

图片来源:君实生物公告
根据公告,本次许可与商业化协议的签署是君实生物持续拓展全球商业化网络的重要实践,并将加快特瑞普利单抗及其他产品在海外市场的开拓。
内卷市场水深火热,
特瑞普利表现如何?
作为国产PD-1的代表,特瑞普利单抗在群雄逐鹿的市场中一直在稳步前进。
在适应症扩展方面,根据药智数据,特瑞普利单抗已有黑色素瘤、鼻咽癌、尿路上皮癌等多项适应症获批。四月初,特瑞普利单抗用于可手术非小细胞肺癌患者围手术期治疗还获得了药监局受理。
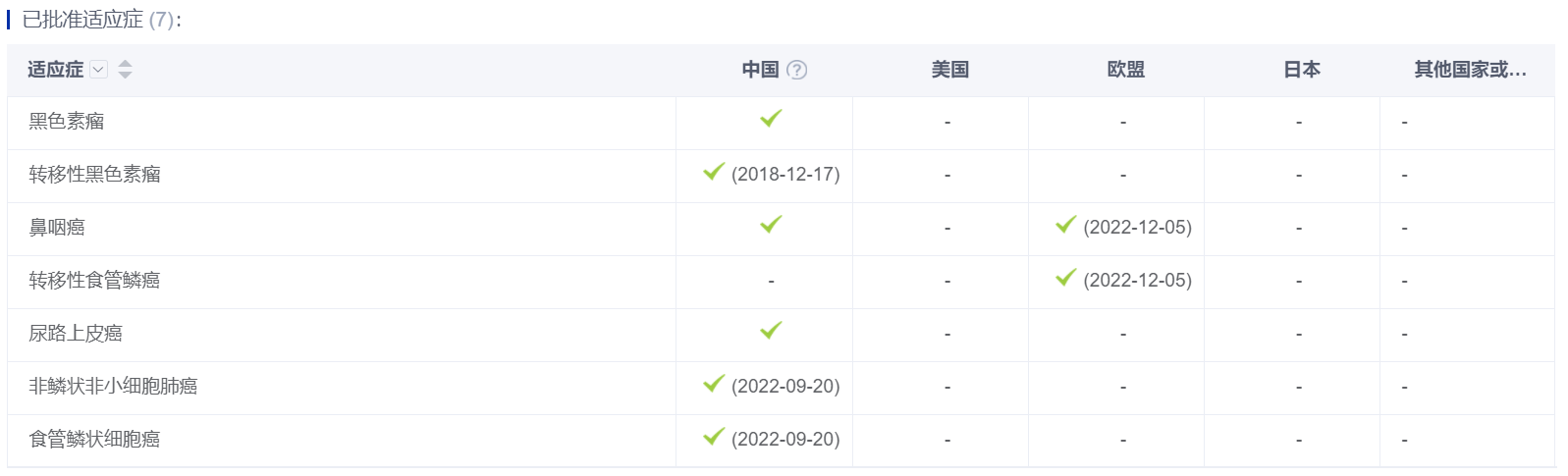
图片来源:药智数据——全球药物分析系统
然而在全球商业化方面,虽然君实已对特瑞普利单抗开展了覆盖超过15个适应症的30多项临床研究,但是其目前在海外获批的适应症并不多,甚至尚无任何适应症获得了FDA的批准。
而观察国内的PD-1形式,只能用“内卷”来形容。除了赛道拥挤,不断有“后浪”袭来,还有医保的“拍打”,导致药物降价而难以收回成本。
据君实2022年年报,特瑞普利单抗在国内市场实现销售收入7.36亿元,同比增长78.77%。但是仅截至2021年,特瑞普利单抗的累计研发投入都已达到了36.79亿元。
也就是说,对特瑞普利单抗而言,就连实现收支平衡都很困难。
由此,“出海”成为了必然的下一步。
出海之路道阻且长,
特瑞普利卷到何地?
早在2021年3月,君实生物便已向FDA滚动提交了特瑞普利单抗用于治疗复发或转移性鼻咽癌的上市申请。但是受疫情阻碍,被搁置。
2022年07月,君实生物重新提出上市申请。目前特瑞普利单抗已在黏膜黑色素瘤、鼻咽癌、软组织肉瘤、食管癌及小细胞肺癌领域获得了FDA授予的2项突破性疗法认定、1项快速通道认定、1项优先审评认定和5项孤儿药资格认定。
可以说,论实力,特瑞普利单抗绝对靠谱。
但是,在欧美市场,PD-1只会更卷。想要在此杀出一条大路,只会更难。
于是转身向东南亚走去。
3月底,君实生物发布公告,授予康联达生技全资子公司Excellmab在泰国、文莱、柬埔寨、印尼、老挝、马来、缅甸、菲律宾及越南,开发和商业化静脉注射用特瑞普利单抗的独占许可及其他相关权利。
1个多月后,就在昨天,君实又与瑞迪博士实验室达成协议,将特瑞普利单抗扩张至巴西、墨西哥、哥伦比亚、阿根廷等地区。
在这个过程中,君实收获不少。虽然未来仅会得到特瑞普利单抗在这些地区的一部分销售额,但是若商业化及销售由君实全权负责,或许会更费力,最终也不见得能收获更多。
小结
君实生物表示,这次协议是持续拓展全球商业化网络的重要实践,将会加快对其他药物的出海。实际上,特瑞普利单抗的路都是靠“质量”走出来的,没有好的疗效,谁愿意买单?所以归根究底,除了商业战略,能做出优异的“firstinclass”才是硬道理。
声明:本文系神州医药网转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!
推荐资讯
神州医药热门单品推荐

- 2024第五届西藏医疗器械及大健康产业展览会
- 主要产品:
- 热度:

- 了解详情

- 2024香港国际生物科技展览暨论坛
- 主要产品:
- 热度:

- 了解详情

- 2024第32届广州国际大健康产业博览会
- 主要产品:
- 热度:

- 了解详情

- 2026第35届【北京】中国国际健康产业博览会
- 主要产品:
- 热度:

- 了解详情

- 2026第20届上海国际养老与辅具及康复医疗博览会(AID老博会)
- 主要产品:
- 热度:

- 了解详情
- 医药资讯
- 涨超120%的皮炎明星药,17家药企竞逐国产第3家
- 获批!国产改良型新药,登陆美国
- 又一1类新药获批上市!销售收入有望超60亿
- 彭水俊苗山医药研究院
- 今年1—7月,职工医保个账家庭共济金额达227亿元
- 关于做好2024年城乡居民基本医疗保障有关工作的通知
- 中药面包、中药冰淇淋…是养生还是智商税?专家提醒
- 十八次方干膜上市
- 国家卫健委:全面推进紧密型县域医共体建设
- 国家药监局综合司关于印发药品监管人工智能典型应用场景清单的通知

网站备案号:琼ICP备2022001664号-24 增值电信业务经营许可证:琼B2-20221748
神州医药网郑重提示:本网站只起到信息平台作用,不对交易行为负担任何责任,请自行核实,谨慎行事。
任何单位及个人不得发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息。
联系电话:400-101-5699 手机:18815323799(同微信)(只提供招商信息服务,不卖药) 客服微信/QQ:3331677131 邮箱:shenzhouyibo@126.com
 琼公网安备46010002000141号
琼公网安备46010002000141号
























点击留言(留言后专人第一时间快速对接)
已有 1826 企业通过我们找到了合作项目